Hace no mucho os contamos que el litifilimab superaba con éxito la fase II del ensayo clínico para el tratamiento del lupus cutáneo.
Con fecha 8 de septiembre, se han publicado los resultados de este mismo estudio para el tratamiento del lupus eritematoso sistémico, que también han sido exitosos en la mejora de los problemas articulares tan comunes entre los pacientes afectados de esta enfermedad.
¿Qué es el litifilimab?
El litifilimab es un anticuerpo monoclonal humano dirigido contra el BDCA2, uno de los receptores de las células dendríticas plasmacitoides, la principal fuente de interferón de tipo I (INF-I).
Vamos por partes para entenderlo bien.
- Es un anticuerpo monoclonal, esto es, una molécula muy selectiva que se va a “pegar” a una diana molecular muy concreta. Está dentro de los llamados “fármacos biológicos”.
- Esta diana es el BDCA2, que es un receptor celular. Los receptores son como unos interruptores que activan o desactivan procesos en la célula. Cuando se activa este BDCA2 por estímulos concretos, se manda una señal y empiezan a pasar cosas dentro de la célula…
- En este caso, hablamos de células dentríticas plasmocitoides. Si olvidamos el nombre, son un tipo de células que forman parte de nuestras defensas. Una de sus labores es producir interferón y otras sustancias (citoquinas y quimocinas) que activan la inflamación. Recordemos que los interferones son uno de los tipos de citocinas, las proteínas proinflamatorias generadas por nuestro sistema inmune ante una infección.
Las células dendríticas son uno de los muchos tipos de células que intervienen en la respuesta inmunitaria a través de la presentación del antígeno a los linfocitos T, que se activan, secretando más citocinas y activando, a su vez, otras respuestas inmunitarias.
Por tanto, la idea final es que el litifilimab se pegue al BDCA2 y lo bloquee, disminuyendo la producción de IFN-I, citoquinas inflamatorias y quimocinas.
Si frenamos la producción de fuego, será menos probable que tengamos un incendio, ¿verdad?
Pues ésta es la lógica de usar este fármaco.
¿En qué consistió el ensayo clínico?
Nuestra idea puede ser muy buena.
Pero la realidad es muy complicada y tenemos que demostrar que esa magnífica idea, la de bloquear ese receptor concreto con nuestro fantástico aniticuerpo efectivamente sirve para controlar el lupus.
Para eso se hacen los ensayos clínicos, con cuatro fases bien diferenciadas.
Este estudio en fase II, llamado TOPAZ-1 y TOPAZ-2, evalúa la eficacia y seguridad del litifilimab en pacientes adultos con lupus eritematoso sistémico que estén recibiendo terapia estándar, excluyendo los tratamientos biológicos.
Es decir, a pacientes ya tratados con fármacos convencionales pero que no acaban de estar bien se les propone añadir este fármaco y ver dos cosas:
- Si es seguro o los efectos secundarios son graves o limitantes
- Si es eficaz y realmente mejora el lupus.
Como “mejorar el lupus” es algo muy ambiguo e inespecífico, en los ensayos se determinan objetivos concretos y medibles. En este caso, por ejemplo, nos podríamos plantear “número de articulaciones con dolor y/o inflamación”. Esto es un indicador medible por cualquiera y que nos permite evitar subjetividades.
El ensayo clínico en fase II se diseñó en dos partes: en una de ellas se evaluó el litifilimab en pacientes con lupus eritematoso sistémico (LES) y en otro, en pacientes con lupus eritematoso cutáneo (LEC).
Los resultados en LEC se publicaron el pasado 28 de julio. Puedes leer sobre ello en el artículo que ya publicamos y que os dejamos al final del artículo.
Esta vez, os hablamos del ensayo clínico en LES, en el que participaron 120 pacientes con 4 o más articulaciones con dolor e inflamación que fueron aleatorizados en dos grupos: el primero, de 64 pacientes, recibió 450 mg de litifilimab mientras que el otro, de 56 pacientes, recibió un placebo (algo que parece un fármaco y que se presenta idéntico al original pero que no lo es)
El tratamiento (o placebo) se administró en las semanas 0, 2, 4, 8, 12, 16 y 20.
¿Cuáles fueron los resultados del estudio?
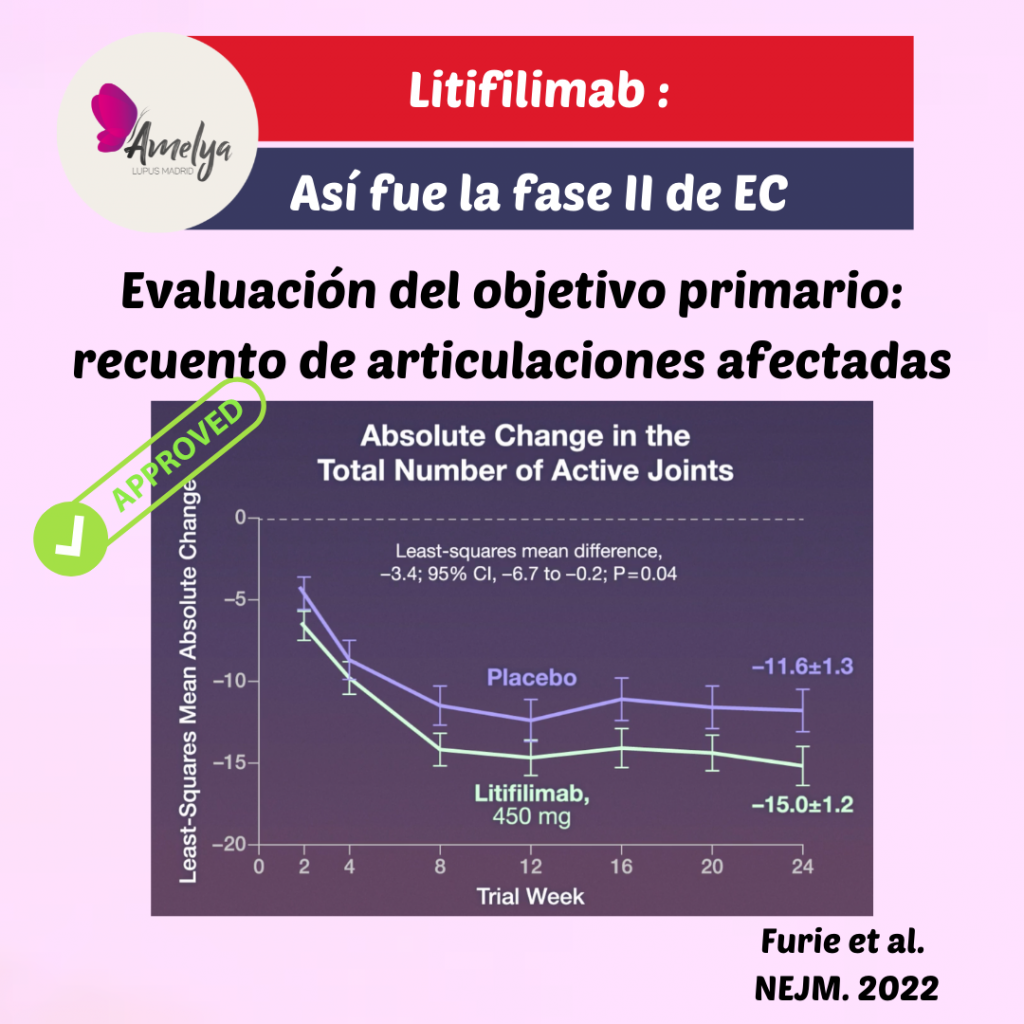
En la semana 24 se evaluó si se había alcanzado el objetivo primario: el cambio en el recuento de articulaciones afectadas. Se observó que los pacientes que habían recibido litifilimab habían experimentado una mejora mayor respecto a los que habían recibido placebo.
Dicha mejoría consistió en una mayor reducción en el número de articulaciones inflamadas y con dolor de los pacientes que recibieron litifilimab, en comparación con los que recibieron placebo.
En relación con los efectos adversos observados, se dieron aproximadamente en el 60% de los pacientes de cada grupo y fueron en su mayoría leves o moderados. Se dieron 2 casos de herpes zóster y un caso de queratitis herpética.
Se dieron efectos adversos graves en el 5% de los pacientes que recibieron litifilimab y en el 11% de los que recibieron placebo, lo que no deja de ser muy llamativo, dicho sea de paso.
En cuanto a los efectos adversos más comunes, estos fueron diarrea, nasofaringitis, infecciones del tracto urinario, caídas y dolor de cabeza.
A pesar de las limitaciones del estudio, estos buenos resultados apoyan la realización de un estudio en fase III en la que se evaluará la eficacia y seguridad del litifilimab pero a una escala mucho mayor, con más pacientes dado que se ha demostrado seguridad y eficacia.
La investigación en el lupus
La investigación lleva su tiempo y pasan muchos años desde que se descubre una molécula hasta que las autoridades sanitarias dan la aprobación para su comercialización.
Como curiosidad, este ensayo clínico en fase II comenzó el 20 de octubre de 2016 y concluyó el 18 de noviembre de 2019. Y es ahora cuando se han publicado los resultados.
Si hablamos de ensayos clínicos en lupus, es más complicado aún, ya que, debido a la heterogeneidad del lupus y otros factores, muchos de los ensayos clínicos no llegan a superar la fase III. Un ejemplo de esto es el ustekinumab, de cuyo fracaso ya os hablamos hace un tiempo.
Sin embargo, queremos transmitiros las palabras del investigador principal de este estudio, el Dr. Richard Furie: «el futuro es prometedor. Hay muchos tratamientos que se están desarrollando en lupus y finalmente estamos viendo éxitos”
Artículos relacionados:
- El litifilimab pasa a la fase III de pruebas para el tratamiento del lupus cutáneo.
- El ustekinumab no supera la fase III del ensayo clínico.
- Más noticias sobre lupus, aquí: https://lupusmadrid.org/noticias/
Fuentes:
- Richard A. Furie et al. Trial of Anti-BDCA2 Antibody Litifilimab for Systemic Lupus Erythematosus. N Engl J Med 2022; 387:894-904 DOI: 10.1056/NEJMoa2118025.
Licenciada en Economía y autora del blog Tu Lupus Es Mi Lupus.
EUPATI fellow.
Community manager en Lupus Europe, AMELyA Lupus Madrid, ACOLU Lupus Córdoba y SAF España.
Redactora web en AMELyA Lupus Madrid y en SAF España.
-
Escrito por Nuria Zúñiga Serranohttps://lupusmadrid.org/author/nuria-zuniga/
-
Escrito por Nuria Zúñiga Serranohttps://lupusmadrid.org/author/nuria-zuniga/
-
Escrito por Nuria Zúñiga Serranohttps://lupusmadrid.org/author/nuria-zuniga/
-
Escrito por Nuria Zúñiga Serranohttps://lupusmadrid.org/author/nuria-zuniga/

El Dr. Rascón es licenciado en Medicina y Cirugía por la Universidad Autónoma de Madrid y especialista en Medicina Interna vía MIR en el Hospital Son Dureta.
Posee un máster en Manejo Clínico de Enfermedades Autoinmunes (Universidad de Barcelona) y otro máster en Gestión Clínica de Unidades Asistenciales (Universidad Juan Carlos I de Madrid).
Además, es miembro de la Sociedad Catalanobalear de Medicina Interna y de la Asociación de Salud Digital.
-
Revisado por el Dr. Francisco Javier Rascón#molongui-disabled-link
-
Revisado por el Dr. Francisco Javier Rascón#molongui-disabled-link



